與AlphaFold3持平!國產抗體設計生成式AI大模型發布,能同時預測抗原抗體復合物結構和抗體從頭設計
AlphaFold3引起的浪潮下,一個新的抗體設計生成式AI大模型浮出水面。
名為GeoFlow,能夠同時用于抗原-抗體復合物結構預測和抗體從頭設計。
例如,給定抗原結構和特定表位,GeoFlow能夠生成全新的抗體分子:

△基于GeoFlow的抗體從頭生成示意圖
在抗原-抗體復合物結構預測任務上,在由66個抗原-抗體復合物結構構成的測試集上,GeoFlow的Top-1成功率達43.9%,與AlphaFold3持平。
GeoFlow研發團隊來自生成式AI驅動的蛋白質設計研發平臺公司——百奧幾何,百奧幾何由AI藥物發現科學家唐建博士于2022年創立,AI三巨頭之一、圖靈獎獲得者Yoshua Bengio擔任首席科學顧問。
近日,由Google DeepMind和Isomorphic Labs等團隊開發的AlphaFold3登上Nature,引發了業界廣泛關注。
與上一代方法相比,AlphaFold3將預測的范圍擴充到了幾乎所有的生命分子以及它們之間的相互作用,是生成式AI在生命科學領域的又一重要里程碑。
其模型的最大創新點之一,是用上了大火的生成式AI模型——擴散模型(AlphaFold 2為判別式AI模型),直接生成每個原子的3D坐標。
如果說傳統的判別式AI是樂評人,可以對一首歌的節奏、風格、編曲進行識別和評價,那么生成式AI就是歌手,可以創作出新的作品。
從評價數據到生成數據,AI的應用場景得到了極大的拓展。例如,在結構預測場景中,生成式AI能更快地采樣到更多的構象;在蛋白設計場景中,生成式AI能更高效地探索蛋白空間,設計具有預期功能的復雜蛋白分子。
擴散生成模型早期主要用于圖像生成(近期也被用于三維視頻的生成,如Sora)。
百奧幾何的核心團隊,2021年起將擴散模型用于分子的三維結構生成,曾發GeoDiff論文是2022年AI領域引用量排名前50的論文之一。
基于前期技術積累,他們研發了最新的生成式AI抗體設計大模型GeoFlow。
GeoFlow模型架構圖如下:
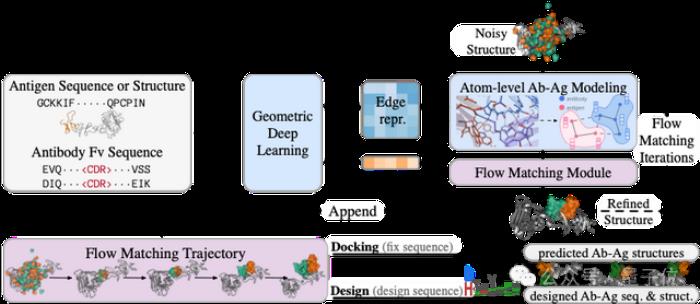
GeoFlow基于幾何深度學習架構和最新的流匹配生成模型(flow matching),能夠同時用于:
在原子層面對抗原-抗體相互作用力進行建模是這兩項任務的核心難點。
與現有的Transformer架構不同,GeoFlow采用了幾何深度學習基礎模型,能夠更好地在三維空間上對原子-原子之間的關系進行建模。
在生成模型選擇上,GeoFlow采用了最新的流匹配模型。與擴散生成模型相比,流匹配生成模型的訓練和推理更高效,也更魯棒。
對于GeoFlow的性能,研究團隊在抗原-抗體復合物結構預測任務上進行了測評。
抗原-抗體復合物結構預測在抗體藥物的發現中扮演著至關重要的角色。然而,無論是基于能量函數的傳統方法(如HDock和MOE),還是基于深度學習的預測模型(如AlphaFold 2 Multimer),準確度目前都不太理想。
在由66個抗原-抗體復合物結構(2023年后發布的)構成的測試集上,GeoFlow模型的Top-1成功率(模型打分最高結構的DockQ水平為“Acceptable”以上則視為成功)達到了43.9%,與AlphaFold3持平,大約是AlphaFold2 Multimer的兩倍。
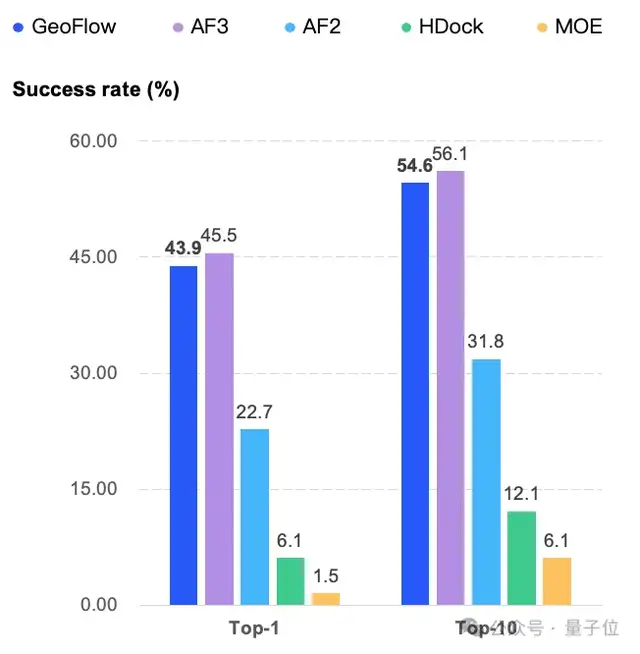
△抗原-抗體復合物預測評測結果
傳統的分子對接方法盡管也能生成多個可能的結構,但打分準確率較低,實際應用的價值相當有限。
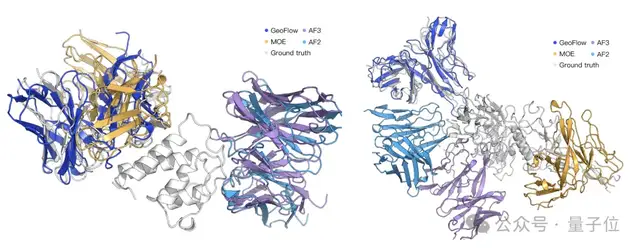
△PDB 8BLQ(左)、8DOK(右)各模型預測結果對比
與AlphaFold3相比,GeoFlow不僅能夠用于抗原-抗體復合物結構預測,還能夠用于抗體的從頭設計和優化。
對于傳統AI方法來說,大分子從頭設計非常困難。主要原因是難以快速采樣高質量的樣本,只能通過判別模型從浩瀚的分子空間中評估大量低質量樣本,這個過程如同大海撈針。
生成式AI的出現為大分子設計帶來了革命性的機遇。
以HER2靶點為例,基于上市的抗體藥物Herceptin的結合表位,研究團隊利用GeoFlow生成了一個小的抗體庫,然后再利用噬菌體庫進行篩選。在得到的十條候選序列中:
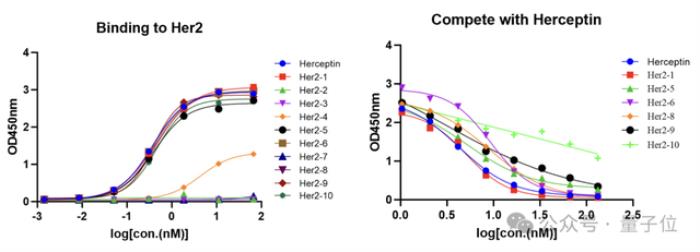
上述結果展現了生成式AI在大分子從頭設計領域的應用前景。
百奧幾何是一家生成式AI驅動的蛋白質設計研發平臺公司,由AI科學家唐建博士于2022年創立,AI之父、圖靈獎獲得者Yoshua Bengio擔任首席科學顧問。
公司業務主要是通過打造AIGC大模型理解生命語言,搭建自然語言與蛋白質語言多模態大模型,重新構建蛋白質藥物發現及設計過程,打造可編程的蛋白質,應用于生物醫藥和生物制造。
百奧幾何的生成式AI大模型,目前已覆蓋了大分子設計、篩選和改造等環節,并開發了GeoBiologics一站式抗體發現平臺。
目前GeoFlow模型已開放,可用于抗原-抗體復合物結構預測的非商用測試,每周支持預測八個復合物,每個任務輸入支持1150個氨基酸。
- 免責聲明
- 本文所包含的觀點僅代表作者個人看法,不代表新火種的觀點。在新火種上獲取的所有信息均不應被視為投資建議。新火種對本文可能提及或鏈接的任何項目不表示認可。 交易和投資涉及高風險,讀者在采取與本文內容相關的任何行動之前,請務必進行充分的盡職調查。最終的決策應該基于您自己的獨立判斷。新火種不對因依賴本文觀點而產生的任何金錢損失負任何責任。





 新火種
2024-06-11
新火種
2024-06-11 






