像拼樂高一樣設(shè)計新藥,EPFL、牛津團隊AI方法精確設(shè)計優(yōu)化分子3D結(jié)構(gòu)

編輯 | 2049
想象一下,如果開發(fā)一款新藥就像積木搭建一樣,可以自由組合不同的分子部件,并準(zhǔn)確預(yù)測它們與目標(biāo)蛋白質(zhì)的結(jié)合效果。這聽起來可能很科幻,但最新發(fā)表的研究讓這一愿景更近了一步。
瑞士聯(lián)邦理工學(xué)院(EPFL)、劍橋大學(xué)、康奈爾大學(xué)、牛津大學(xué)的聯(lián)合研究團隊開發(fā)的AI系統(tǒng) DiffSBDD ,就像是一位經(jīng)驗豐富的分子建筑師,能夠精確設(shè)計和優(yōu)化藥物分子的 3D 結(jié)構(gòu)。
該研究以「Structure-based drug design with equivariant diffusion models」為題,于 2024 年 12 月 9 日發(fā)布在《Nature Computational Science》。

新藥研發(fā)是一個極其耗時和昂貴的過程。傳統(tǒng)方法通常需要科學(xué)家從數(shù)百萬個候選分子中篩選,就像在大海中尋找針一樣。即使找到了有潛力的分子,還需要經(jīng)過漫長的優(yōu)化過程。更重要的是,現(xiàn)有的 AI 輔助方法往往過于專一,缺乏靈活性。因此,能否找到一種更靈活、更高效的方法,正成為業(yè)界和學(xué)術(shù)界共同關(guān)注的焦點。
技術(shù)創(chuàng)新:SE(3)- 等變擴散模型的工作原理
DiffSBDD 的核心創(chuàng)新在于將 SE(3)- 等變擴散模型引入結(jié)構(gòu)導(dǎo)向的藥物設(shè)計中。該方法將藥物設(shè)計轉(zhuǎn)化為一個三維條件生成問題,通過引入 SE(3)- 等變性來處理分子系統(tǒng)中的自然對稱性,包括旋轉(zhuǎn)和平移,但特意排除了不可疊加的轉(zhuǎn)換。
這種設(shè)計選擇源于廣泛研究的藥物立體化學(xué)案例。如抗抑郁藥citalopram(圖1e)具有兩種對映異構(gòu)體,但只有S型具有所需的治療效果。這種異構(gòu)體間的差異只能通過反射敏感的模型來檢測,證明了 SE(3)- 等變性在手性藥物設(shè)計中的重要性。從這一原理可見,分子立體結(jié)構(gòu)的細(xì)微差異對藥效影響巨大,正是 DiffSBDD 發(fā)力之處。
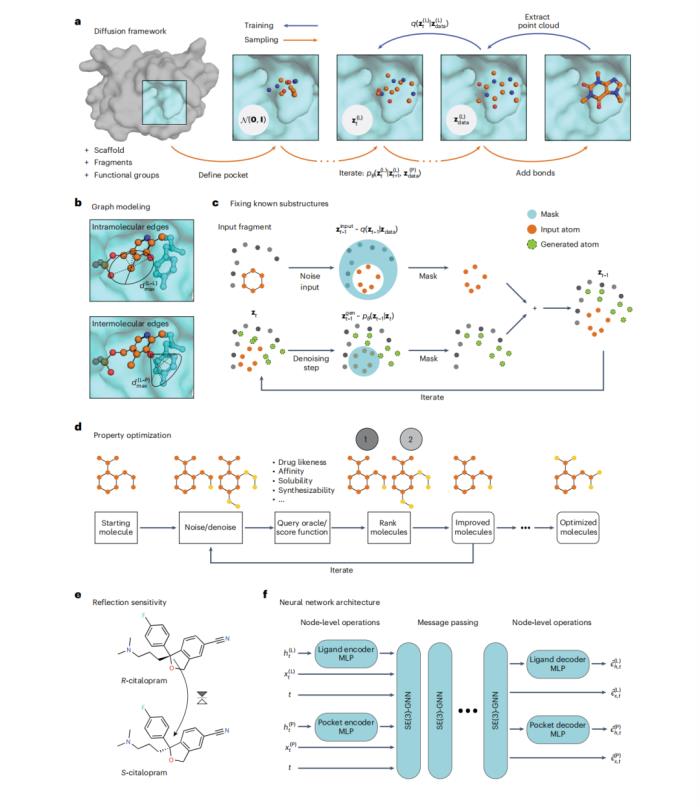
DiffSBDD的工作流程可分為兩個主要階段:
訓(xùn)練階段
在訓(xùn)練過程中,擴散過程 q 對原始原子點云進行噪聲處理,生成不同時間步長的噪聲版本。神經(jīng)網(wǎng)絡(luò)模型學(xué)習(xí)近似這個逆過程,以目標(biāo)蛋白質(zhì)結(jié)構(gòu)作為條件。一旦訓(xùn)練完成,初始噪聲點云從高斯分布中采樣,并使用學(xué)習(xí)的轉(zhuǎn)移概率逐步去噪。最后在生成過程末尾添加共價鍵。完成上述訓(xùn)練后,系統(tǒng)便能為后續(xù)的條件生成打下堅實基礎(chǔ),讓分子去噪過程更加精準(zhǔn)。
條件生成階段
針對蛋白質(zhì)口袋的 3D 生成模型,研究團隊提出了兩種不同方法:
1、DiffSBDD-cond: 在去噪過程中保持蛋白質(zhì)口袋環(huán)境不變。
2、DiffSBDD-joint: 先學(xué)習(xí)配體-口袋對的聯(lián)合分布,推理時再引入目標(biāo)口袋信息。
兩種方法在CrossDocked和Binding MOAD測試集上均表現(xiàn)優(yōu)異,生成的分子具有與參考分子相當(dāng)或更好的結(jié)合得分。以人類受體(PDB:6c0b)為例,模型能夠?qū)⒃绢愃幮暂^差(QED=0.36)的長鏈脂肪酸優(yōu)化為具有更好藥物特性(QED=0.87)的分子,通過合理設(shè)計芳香環(huán)和可旋轉(zhuǎn)鍵實現(xiàn)了更優(yōu)的結(jié)合構(gòu)象和熵貢獻。
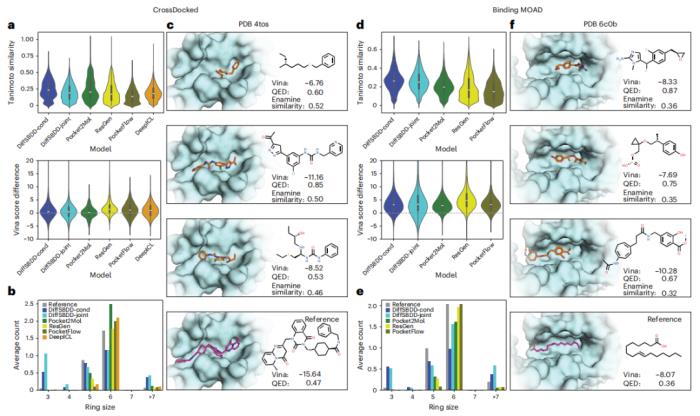
圖 2:評估分布式學(xué)習(xí)能力和生成的實例。(來源:論文)
DiffSBDD 的多功能分子設(shè)計能力
DiffSBDD 展現(xiàn)出在藥物研發(fā)中的通用性和靈活性,無需為每個具體任務(wù)重新訓(xùn)練模型就能勝任多項關(guān)鍵任務(wù)。正是在這些多樣化場景中的成功應(yīng)用,印證了它作為“通用分子設(shè)計平臺”的潛力。
分子結(jié)構(gòu)設(shè)計能力
在分子片段任務(wù)中,DiffSBDD 展示了多樣的設(shè)計能力。模型能以給定片段為基礎(chǔ)構(gòu)建完整藥物分子,同時可以保留關(guān)鍵功能團并重新設(shè)計分子骨架。一個典型案例是激酶抑制劑(PDB 編號 2gm1)的重設(shè)計,模型在保持結(jié)合活性的同時成功重構(gòu)了分子骨架。在片段合并方面,研究團隊展示了將 SARS-CoV-2 Nsp3 蛋白的兩個片段(PDB 編號 5rsw 和 5rue)成功整合的實驗。
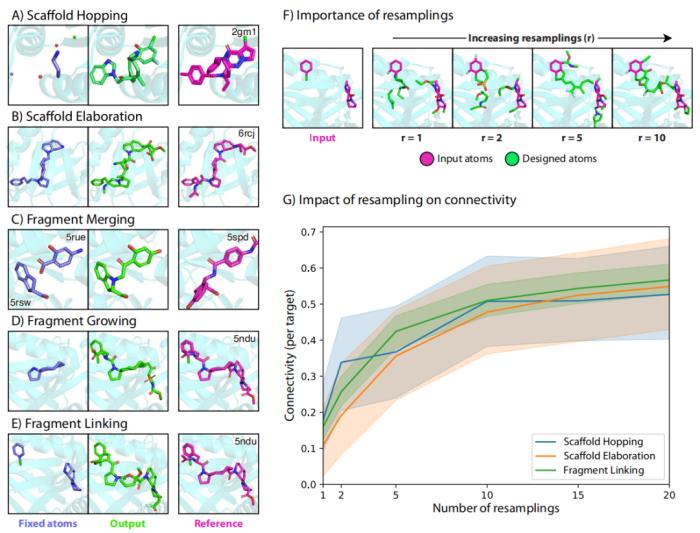
圖 3:分子著色結(jié)果。(來源:論文)
選擇性優(yōu)化與多屬性調(diào)控
在激酶抑制劑優(yōu)化的案例中,DiffSBDD 展示了其多目標(biāo)優(yōu)化能力。模型通過五輪優(yōu)化,將分子對目標(biāo)激酶 BIKE(PDB 編號 4w9w)的結(jié)合得分從 -7.2 提升至 -13.9,同時降低了對非目標(biāo)激酶 MPSK1(PDB 編號 2buj)的結(jié)合傾向,從 -10.8 降低至 -8.7。除了選擇性優(yōu)化外,模型還能同時調(diào)控多個藥物屬性,包括類藥性(QED,從 0.35 提升至 0.54)、合成可行性(SA score)、結(jié)合親和力(Vina score)等關(guān)鍵物理化學(xué)性質(zhì)。
這種多功能性源于模型的兩個關(guān)鍵創(chuàng)新:首先是其通用性,一個預(yù)訓(xùn)練模型即可應(yīng)用于廣泛的問題范圍;其次是設(shè)計約束的靈活性,能夠同時處理現(xiàn)成屬性優(yōu)化、顯式負(fù)向設(shè)計和部分分子設(shè)計等多種任務(wù)。如原文所述「While we provide empirical results for only our model, the methodology can be readily used in combination with other recently published diffusion models for small-molecule design」這種方法學(xué)的普適性為藥物研發(fā)提供了新的可能性。
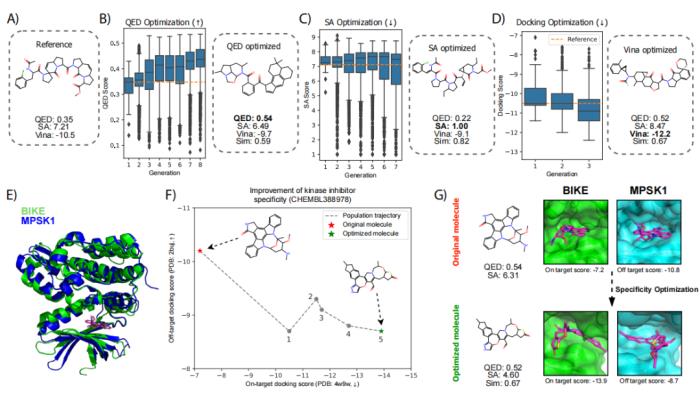
圖 4:使用 DiffSBDD 進行分子優(yōu)化的結(jié)果。(來源:論文)
局限性與未來展望
盡管 DiffSBDD 展現(xiàn)出強大的藥物設(shè)計潛力,研究團隊也坦言仍面臨挑戰(zhàn):純從頭設(shè)計(de novo design)難度較大,常因樣品質(zhì)量和可合成性受限而阻礙實驗驗證。研究表明,在真實亞結(jié)構(gòu)(如片段或支架)范圍內(nèi)進行設(shè)計往往成效更佳,并可借助保留先前合成分子的關(guān)鍵片段來簡化化學(xué)合成和測試。
與以往針對特定任務(wù)訓(xùn)練的專用模型不同,DiffSBDD 通過修改采樣過程即可勝任多項子任務(wù),只需持續(xù)優(yōu)化主模型的分布學(xué)習(xí)和樣本質(zhì)量便能整體提升性能。隨著這項技術(shù)不斷成熟,我們或許正邁向更智能化、個性化的藥物研發(fā)時代,借由其靈活探索分子空間的能力,為精準(zhǔn)醫(yī)療打開新的大門。
論文鏈接:
- 免責(zé)聲明
- 本文所包含的觀點僅代表作者個人看法,不代表新火種的觀點。在新火種上獲取的所有信息均不應(yīng)被視為投資建議。新火種對本文可能提及或鏈接的任何項目不表示認(rèn)可。 交易和投資涉及高風(fēng)險,讀者在采取與本文內(nèi)容相關(guān)的任何行動之前,請務(wù)必進行充分的盡職調(diào)查。最終的決策應(yīng)該基于您自己的獨立判斷。新火種不對因依賴本文觀點而產(chǎn)生的任何金錢損失負(fù)任何責(zé)任。





 新火種
2024-12-28
新火種
2024-12-28 






