探索蛋白質動態變化,新AI方法JAMUN比標準MD模擬更快、更準確

編輯 | 白菜葉
蛋白質結構的動態變化對于理解其功能和開發靶向藥物治療至關重要,尤其是對于隱蔽的結合位點。然而,現有的生成構象集合的方法存在效率低下或缺乏通用性的問題,無法在訓練系統之外發揮作用。
分子動力學 (MD) 模擬是當前探索蛋白質運動的標準,但計算成本高昂,且受短時間步長要求的限制,因此難以捕捉較長時間尺度上發生的更廣泛蛋白質構象變化。
Prescient Design 和Genentech的研究人員推出了 JAMUN(walk-Jump Accelerated Molecular ensembles with Universal Noise),這是一種新穎的機器學習模型,旨在通過實現對蛋白質構象集合的有效采樣來克服這些挑戰。
該研究以「JAMUN:Transferable Molecular Conformational Ensemble Generation with Walk-Jump Sampling」為題,于 2024 年 10 月 18 日發布在 arXiv 預印平臺。

JAMUN 將 Walk-Jump Sampling(WJS)擴展到 3D 點云,代表蛋白質原子坐標。通過利用 SE(3) 等變去噪網絡,JAMUN 可以以比傳統 MD 方法或當前基于 ML 的方法高得多的速度對任意蛋白質的玻爾茲曼分布進行采樣。
JAMUN 還表現出了顯著的轉移到新系統的能力,這意味著它甚至可以為不屬于其訓練數據集的蛋白質結構生成可靠的構象集合。
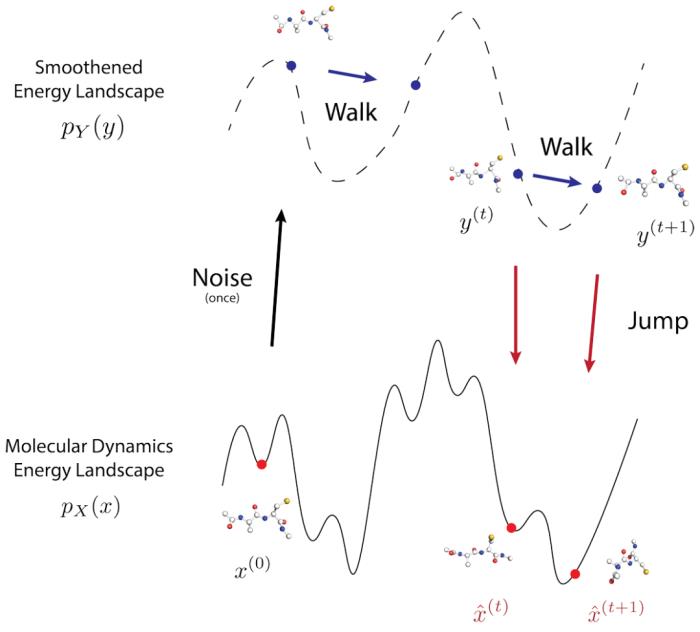
所提出的方法基于「Walk-Jump Sampling」的概念,即將噪聲添加到干凈的數據中,然后訓練神經網絡對其進行去噪,從而實現平穩的采樣過程。
JAMUN 在「Walk」階段采用朗之萬動力學,這已經是分子動力學 MD 模擬中的標準方法。
然后,「Jump」步驟會投射回原始數據分布,從而將過程與每次重新開始分離,而這通常是擴散模型所為。通過分離 Walk 和 Jump 步驟,JAMUN 可以平滑數據分布,足以解決采樣困難,同時保留 MD 數據固有的物理先驗。
JAMUN 是在兩種氨基酸肽的分子動力學模擬數據集上進行訓練的,并成功推廣到未見過的肽。結果表明,JAMUN 可以比標準 MD 模擬更快地對小肽的構象集合進行采樣。
例如,JAMUN 在一小時內計算生成了具有挑戰性的封端肽的構象狀態,而傳統的 MD 方法需要更長的時間來覆蓋類似的分布。
JAMUN 還與可轉移玻爾茲曼生成器 (TBG) 模型進行了比較,展示了顯著的加速和相當的準確性,盡管它僅限于玻爾茲曼模擬而不是精確采樣。
JAMUN 提供了一種強大的新方法來生成蛋白質的構象集合,平衡了效率和物理精度。它能夠以比 MD 快得多的速度生成集合,同時保持可靠的采樣,使其成為蛋白質結構預測和藥物發現應用的有前途的工具。
未來的工作將側重于將 JAMUN 擴展到更大的蛋白質,并改進去噪網絡以實現更快的采樣。
通過利用 Walk-Jump 采樣,JAMUN 朝著可推廣、可轉移的蛋白質構象集合生成解決方案邁出了重要一步,這對于生物學理解和藥物創新都至關重要。
論文鏈接:https://arxiv.org/abs/2410.14621
相關內容:https://www.marktechpost.com/2024/10/21/jamun-a-walk-jump-sampling-model-for-generating-ensembles-of-molecular-conformations/
- 免責聲明
- 本文所包含的觀點僅代表作者個人看法,不代表新火種的觀點。在新火種上獲取的所有信息均不應被視為投資建議。新火種對本文可能提及或鏈接的任何項目不表示認可。 交易和投資涉及高風險,讀者在采取與本文內容相關的任何行動之前,請務必進行充分的盡職調查。最終的決策應該基于您自己的獨立判斷。新火種不對因依賴本文觀點而產生的任何金錢損失負任何責任。





 新火種
2024-11-27
新火種
2024-11-27 






